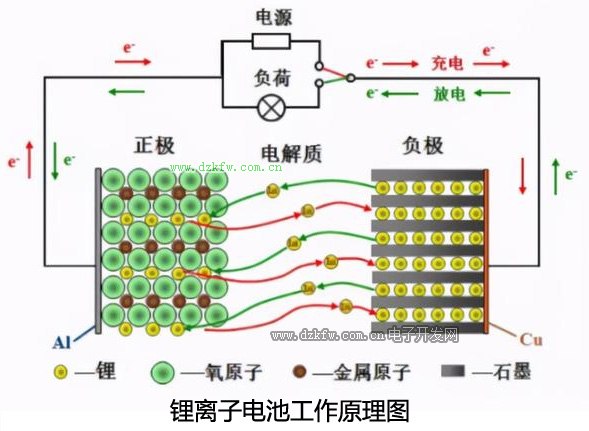
1980年,古迪的夫發明了鈷酸鋰材料,這種材料的結構可以使鋰離子在其中快速移動。以下圖示說明鋰電池的工作原理:
鋰離子電池的反應式C6+LiCoO2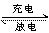 LixC6+Li1-xCoO2(x<1)
LixC6+Li1-xCoO2(x<1)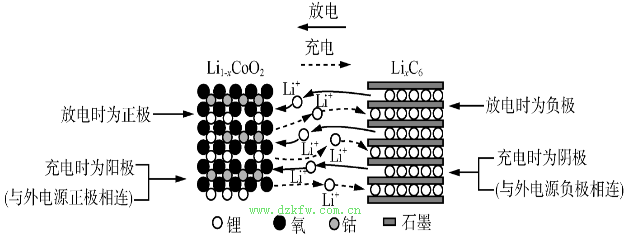
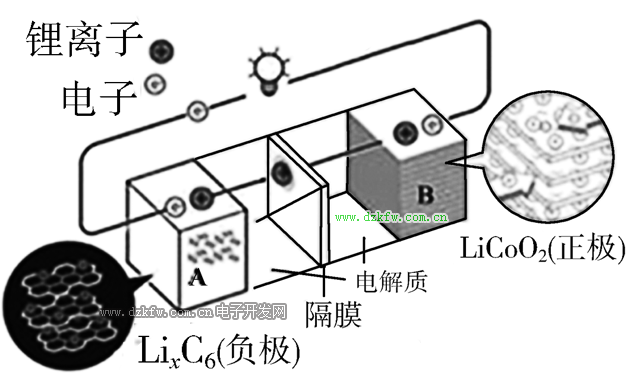
放電時
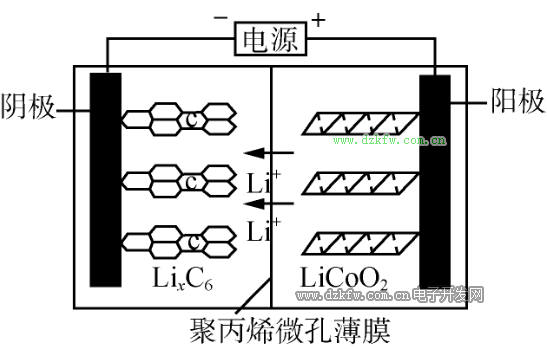
充電時
鋰離子電池工作原理
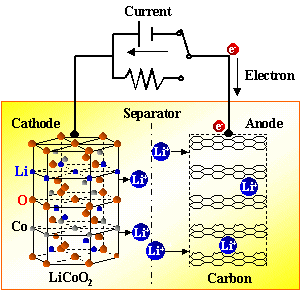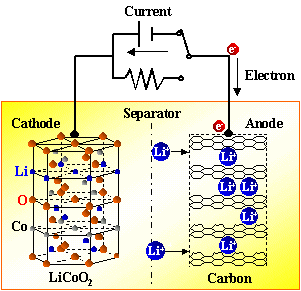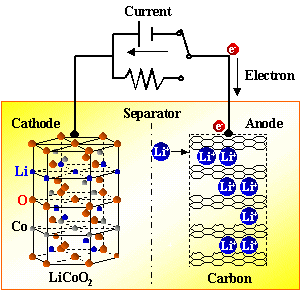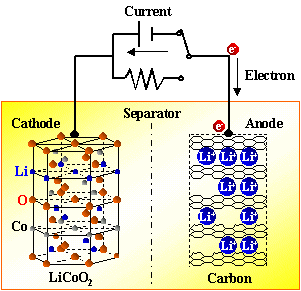
鋰離子電池是一種二次電池(充電電池),它主要依靠鋰離子在正極和負極之間移動來工作。在充放電過程中,Li+ 在兩個電極之間往返嵌入和脫嵌:充電時,Li+從正極脫嵌,經過電解質嵌入負極,負極處于負鋰狀態;放電時則相反。當對電池進行充電時,正極的含鋰化合物有鋰離子脫出,鋰離子經過電解液運動到負極。負極的碳材料呈層狀結構,它有很多微孔,到達負極的鋰離子嵌入到碳層的微孔中,嵌入的鋰離子越多,充電容量越高。當對電池進行放電時(即我們使用電池的過程),嵌在負極碳層中的鋰離子脫出,又運動回正極。回正極的鋰離子越多,放電容量越高。我們通常所說的電池容量指的就是放電容量。


 返回頂部
返回頂部 刷新頁面
刷新頁面 下到頁底
下到頁底